
新闻活动 新闻动态
给纳米药物穿上“细胞外壳”,是近年来仿生纳米技术领域的明星策略。这种细胞膜包覆技术能让纳米材料瞬间获得细胞的“通行证”,在体内穿梭自如。但遗憾的是,这层“外衣”在复杂的体内环境下并不总是稳固,“掉漆”(膜脱落)事件的频发导致纳米药物的治疗效果大打折扣。如何让这层细胞膜穿得更稳、更牢,成为了当前的核心挑战。
近日,西湖大学工学院张越、理学院陈虹宇团队联合加州大学尔湾分校Haleh Alimohamadi团队在Cell Biomaterials期刊上发表了题为“Stabilization of erythrocyte membrane coating on nanoparticle via strong substrate interaction confers enhanced anti-α-hemolysin immunity”的研究。针对细胞膜包覆稳定性低这一长期制约领域发展的核心挑战,研究团队提出“平衡态孵育法”的创新技术方案,通过引入共价耦合策略,通过增强细胞膜与基底纳米材料间的相互作用力,显著提升了膜包覆稳定性(图1)。该研究不仅攻克了细胞膜仿生技术的体内应用瓶颈,更为复杂生理环境下的精准递送奠定了理论与技术基础。
西湖大学理学院博士生黄洁、工学院博士生付涵为本文共同第一作者;张越、陈虹宇与加州大学尔湾分校的Haleh Alimohamadi教授为共同通讯作者。

原文链接:https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(26)00068-1
“平衡态孵育法”与经典的“超声法”有何差别?
1.在天然细胞膜中混入巯基脂质,建立共价界面连接
研究团队另辟蹊径,在红细胞膜中掺杂了含巯基的脂质分子(PSH),PSH末端的巯基可与金纳米颗粒形成共价键(Au-S键),将膜-颗粒相互作用由物理吸附转变为化学键合。
2.添加微量有机溶剂,促进膜融合与铺展
天然红细胞膜流动性较低,在纳米颗粒表面不易完全铺展。团队在组装体系中加入微量有机溶剂乙腈,增强脂质分子流动性,使膜能够充分融合并均匀覆盖于颗粒表面。
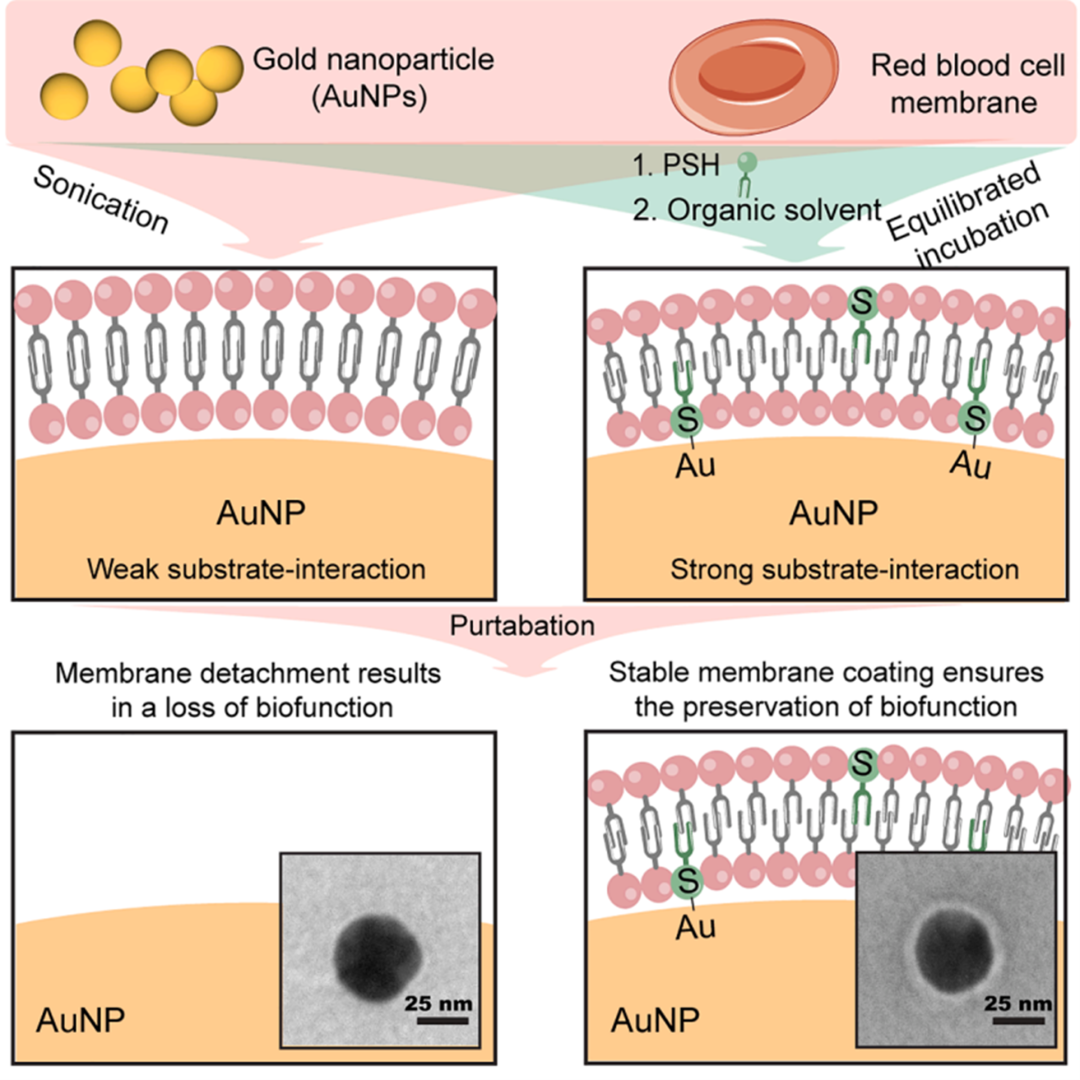
图1. 平衡态孵育法制备红细胞膜包被金纳米颗粒(AuNP@RBCM)
平衡态孵育法适用性广且更“扛得住”
平衡态孵育法在底物适用性和膜包覆稳定性方面均显著优于传统超声法。透射电镜图像显示(图2),对于直径15、40、75 nm的球、棒、三角片及立方颗粒,平衡态孵育法均可形成连续均匀膜层。而传统超声法在75 nm球、三角片和立方颗粒出现明显的裸露区域。这表明,平衡态孵育法通过增加膜流动性克服了高曲率区域膜融合的限制,展现出更广泛的底物适用性。在膜包覆稳定性测试中,面对生理剪切力(1.1-2.2 Pa)的冲击或金黄色葡萄球菌α-溶血素(α-HL)插入细胞膜间的扰动,传统超声法制备的纳米颗粒由于膜层脱落而迅速聚集,平衡态孵育法制备的样品则可保持单分散状态,揭示膜层完整。这证明,平衡态孵育法制备的膜包覆层既能抵抗物理剪切,也能抵御毒素分子的膜扰动。

理论模型解释了稳定性的来源
模型指出膜层稳定性由膜-基底相互作用刚度(Ω)、基线膜张力(λ0)与扰动诱导自发曲率(C)三者共同决定。更强的膜-基底相互作用大幅提升了界面约束刚度,使膜层能够承受更大的由剪切作用或毒素插入引起的膜扰动,从而提高失稳阈值并增强包覆稳定性。
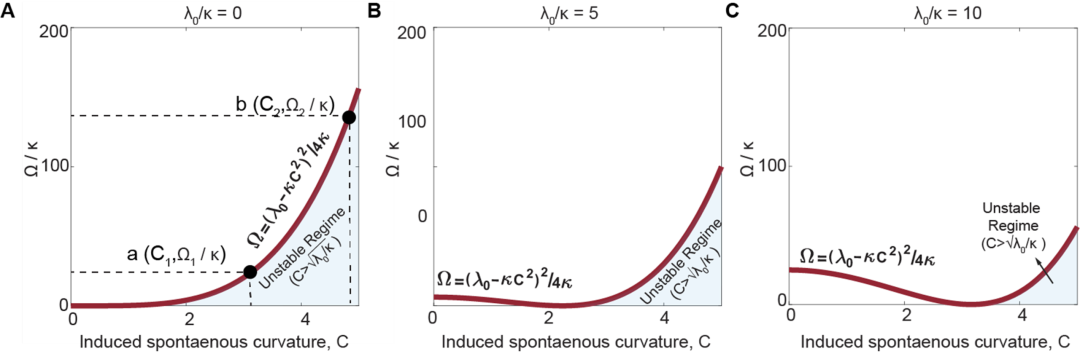
更稳定的包覆,带来更好的疫苗效果
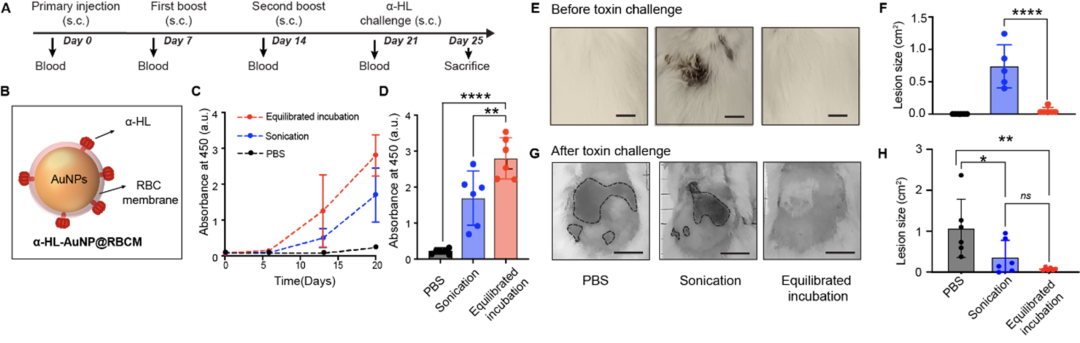
图4. 平衡态孵育法制备的α-HL-AuNP@RBCM疫苗安全性和免疫效果更强
小结
这项研究提出了一种更稳定的细胞膜包覆新策略。通过在细胞膜与纳米颗粒之间构建更强的界面连接,研究团队有效解决了传统方法中膜层易脱落的问题,并在抗α-溶血素疫苗体系中验证了其在递送效率、安全性和免疫保护效果上的优势。这一突破不仅解决了仿生纳米材料的核心技术瓶颈,更为后续这类材料走向临床应用、开发出更有效的治疗方案,打下了坚实的基础。
















