
新闻活动 新闻动态
抗生素耐药性正在逐步削弱现代医学的基础。随着耐甲氧西林金黄色葡萄球菌等多重耐药菌的广泛出现,传统以“单一靶点抑制”为核心的抗生素设计策略正面临结构性瓶颈。新问题并不完全在于缺乏分子来源,而在于既有发现路径的收敛性过强。
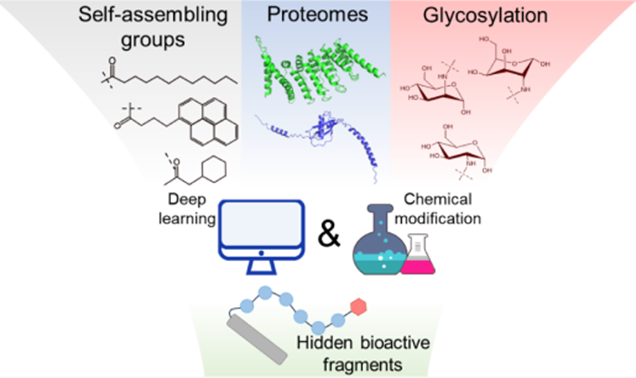
在这一背景下,西湖大学理学院王怀民课题组提出了一种不同于经典药物发现逻辑的思路:不再将蛋白质视为不可拆分的功能单元,而是将其看作潜在功能片段的集合体。这一视角源于生物学中的普遍事实——大量生物活性肽并非独立编码,而是通过蛋白质的受控降解过程被释放并发挥作用。其真正的挑战在于规模,蛋白质组中可能蕴含的短肽片段数量呈指数级增长,传统实验筛选难以覆盖这一空间。为此,王怀民课题组对不同来源的蛋白质序列进行系统分析,重点识别那些既具备抗菌潜力、又具有自组装倾向的片段,结合化学重编程改造。这一策略的关键不在于预测单一功能,而在于将分子尺度的物理行为纳入功能发现框架。
近日,这一结果以“Proteome-Mining and Chemical Activation of Hidden Bioactive Fragments as Antimicrobial Assemblies”为题,发表于JACS。
西湖大学理学院博士后刘华杨与博士研究生徐子衡为文章第一作者,理学院王怀民研究员为文章通讯作者。

论文地址:https://pubs.acs.org/doi/10.1021/jacs.5c20598
实验结果表明,这一“片段挖掘”策略具有高度有效性。大量原本未被注释为抗菌相关的蛋白质序列中,确实蕴含着可转化为功能分子的短肽片段,验证成功率远高于随机筛选。这一结果从方法论层面提示,蛋白质组并非功能已被穷尽的资源,而更像是一座尚未系统开采的功能库。
在具体实例中,王怀民课题组进一步展示了一个极端简化的模型分子:仅由6个氨基酸构成的短肽。在引入疏水基团后,该分子能够在水相环境中自发形成稳定的纳米级组装结构,并通过多价作用与细菌细胞膜发生强烈相互作用。这种基于自组装的抗菌机制,不依赖于精确分子识别,而是通过集体效应实现膜破坏,这一机制在抗耐药性方面具有天然优势。与靶向单一代谢通路的抗生素不同,细胞膜破坏涉及细菌生存的基本物理结构,突变空间受限,耐药进化成本显著提高。然而,膜活性分子往往伴随宿主毒性风险,这也是该类分子长期面临的应用障碍。
通过对分子表面化学的微调,研究人员实现了对膜脂选择性的再编程,使组装体更倾向于作用于细菌膜中特有的脂质组分,而降低对哺乳动物细胞膜的非特异相互作用。这一过程并未破坏自组装结构本身,而是通过调控界面化学性质,实现了功能与安全性的平衡。在动物感染模型中,该分子展现出与临床抗生素相当的抗菌效果,同时在生物被膜清除和炎症调控方面显示出附加优势。更值得注意的是,在重复给药条件下,细菌并未出现显著耐药趋势,进一步印证了其作用机制的稳健性。
从更宏观的角度看,这项工作的价值并不局限于某一候选分子,其贡献在于提出了一种从蛋白质结构连续体中发现功能分子的通用框架:结合计算预测、自组装和化学修饰,在分子层面实现“发现——放大——调控”的闭环。这一范式为抗菌分子之外的功能肽发现,提供了可迁移的方法基础。在抗生素研发逐渐逼近物理和进化边界的当下,这种从蛋白质内部重新审视功能来源的策略,或许代表了一条更具可持续性的探索方向。
该研究得到了国家自然科学基金、西湖大学相关经费的支持。
王怀民课题组研究领域
王怀民课题组主要运用材料化学、化学生物学、细胞/分子生物学等开发设计新型生物功能材料,化学生物学工具、活细胞原位标记和反应等。课题组负责人目前主持多个科研项目,为西湖大学理学院生物材料实验室负责人,同时兼任生命科学学院研究员。
招生招聘
在如下领域招聘博士后及相关科研人员:
生物材料、高分子化学、抗菌材料、水凝胶、肿瘤与免疫相关、神经生物学、基因编辑等
联系方式
课题组网站:
https://www.hm-wanglab.com/
















