
新闻活动 新闻动态
近日,西湖大学理学院化学系邓力教授团队在α-氘代三氟甲基胺的不对称合成领域取得重要突破,团队从反应催化机制出发,指导反应设计与条件优化、合理设计新型的基于金鸡纳碱的betaine催化剂,开发出亚胺异构化‒氘代反应的有机催化合成新策略。该方法以廉价易得的重水(D₂O)为氘源,成功实现了手性及消旋α-氘代三氟甲基胺类化合物的高效、高氘代率制备。
相关研究成果以 “Synthesis of α-Deuterated Trifluoromethylated Amines through Isomerization-Deuteration Reaction of Imines” 为题发表于Journal of the American Chemical Society上(2026, DOI:10.1021/jacs.5c21911)。该研究为药物研发、氘代药物合成和有机合成化学等领域提供了新的技术。
西湖大学理学院助理研究员史广法为文章第一作者,理学院博士研究生许翎为第二作者,邓力教授为文章通讯作者。

论文地址:
https://pubs.acs.org/doi/10.1021/jacs.5c21911
在现代科学研究与生物医药产业中,同位素标记化合物占据着不可替代的核心地位。无论是作为揭示生命奥秘的代谢示踪剂、精准解析药物作用机制的定量分析内标,还是用于改善药物代谢性质的氘代药物核心骨架,这类特殊分子为疾病诊断、新药研发及基础化学机理研究提供了独特的技术手段。其中,氘作为氢的稳定同位素,因 C‒D 键比 C‒H 键键能更高,将其引入药物分子的特定代谢位点,可调控药物的代谢稳定性、优化药代动力学性质、降低毒副作用,氘代药物也因此成为当前医药研发的重要方向。多款氘代药物已上市或正处于临床研发阶段;2017年,FDA批准了首个氘代药物——氘代丁苯那嗪,其于2025年实现了全球销售额22.6亿美元的市场规模,彰显了氘代药物的巨大市场潜力和应用价值。
然而,同位素标记化合物的研发与制备仍面临诸多瓶颈:与结构多样、商业化供应充足的非同位素试剂相比,同位素标记化合物的种类极其有限,且存在价格昂贵、制备困难等问题。更具挑战性的是,绝大多数成熟的传统有机合成方法在面对同位素体系时难以适用,常规反应条件极易导致同位素的流失或交换、难以精准控制同位素位点的引入,使得绝大多数现有的合成工具箱无法直接用于同位素化合物的构建。在此背景下,开发能够兼容简单易得、廉价通用同位素试剂(如重水)的新型合成策略,不仅能打破同位素原料稀缺的现实瓶颈,大幅降低同位素化合物的制备成本,满足生物医药领域的迫切实际需求;同时,这也对有机合成方法学提出了新的科学挑战,要求化学家重新设计反应路径、精准调控反应,以解决同位素引入的选择性与效率问题。因此,发展应用简单易得的同位素试剂来合成多种多样的同位素分子的方法既有重要的现实应用价值又有深远的学术探索意义。
手性胺是药物化学中的重要片段,但手性α-氘代胺类化合物的合成方法仍存在诸多局限,如依赖昂贵的氘源、使用金属催化剂引起的金属残留风险、产物局限于α-芳基氘代胺等问题,极大限制了其应用。而兼具三氟甲基的理化性质调控优势和氘的代谢稳定性提升特点的α-氘代三氟甲基胺的不对称合成更是鲜有报道。
针对这一挑战,邓力课题组基于前期在基于金鸡纳碱的甜菜碱型催化剂催化亚胺异构化反应(Scheme 1B, path a)的研究积累,提出并发展了一种有机催化的不对称异构化‒氘代新策略。该策略以廉价易得的重水(D₂O)为氘源,通过将H/D交换过程精准嵌入亚胺异构化的去质子化‒质子化序列中,构建了“去质子化‒H/D交换‒氘代”的新型反应路径(Scheme 1B, path b),成功实现了三氟甲基亚胺的不对称异构化‒氘代反应。利用该策略,团队首次完成了包括烷基和芳基取代的α-氘代三氟甲基胺的高效不对称合成(Scheme 1B),填补了烷基取代底物合成领域的技术空白。需要指出的是,在三氟甲基亚胺的催化不对称异构化反应中,对映选择性质子转移是一种类分子内的过程,效率极高,且对高立体选择性的获得有决定性的作用(Scheme 1B, path a),要将使用外部氘源的H/D交换步骤高效地插入到去质子化‒质子化过程中且保持高立体选择性极具挑战性。研究团队基于对反应催化机制的分析(Scheme 1B, path b),指导开展反应条件优化与催化剂的精准设计,为反应的成功实现奠定了关键基础。
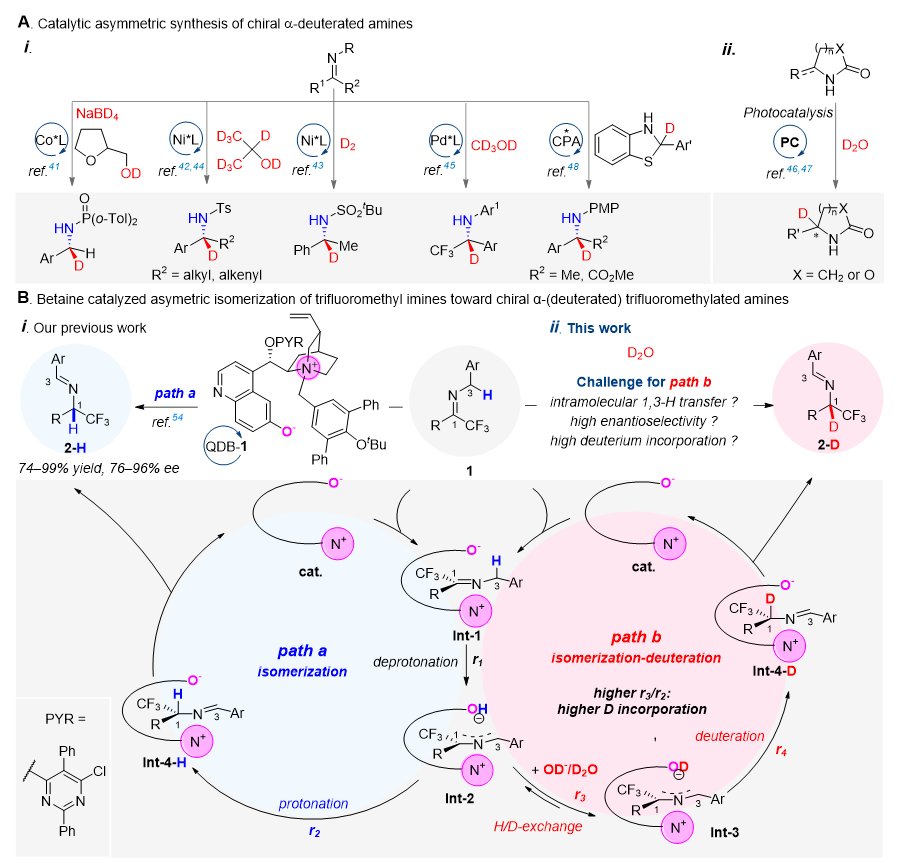
Scheme 1. 手性α-氘代胺的催化不对称合成方法
研究过程中,邓力团队首先通过提高重水的用量和筛选适配的碱,成功地在保持对映选择性的前提下,将甲基-α-氘代三氟甲基胺的氘代率从最初的40%提高到了87%。为进一步提高氘代率,团队针对催化剂结构进行了精准而合理的设计改造。催化剂中6’-OH的pKa和空间位置对去质子化、H/D交换和质子化/氘代步骤的速率都会有影响,因此,通过改变6’-OH的pKa和空间位置设计改造成新型的甜菜碱型催化剂或可在兼顾高对映选择性的情况下取得高氘代率。基于此理念,团队最终发展出一种新型的基于金鸡纳碱的甜菜碱型催化剂,在6’-位通过间羟基苯甲酰基延伸出远程羟基作为质子转移工具,从而实现了脂肪族三氟甲基亚胺的高对映选择性、高氘代率的异构化‒氘代反应。对于一系列的脂肪族三氟甲基亚胺,仅需最低0.2 mol%的催化剂使用量,即可实现89-96%的氘代率、76-94%的ee值和62-82%的分离产率。而通过使用不同构型的催化剂,也可以87-98%的氘代率、79-95%的ee值和57-95%的分离产率得到氘代三氟甲基胺的对映异构体(Table 1)。
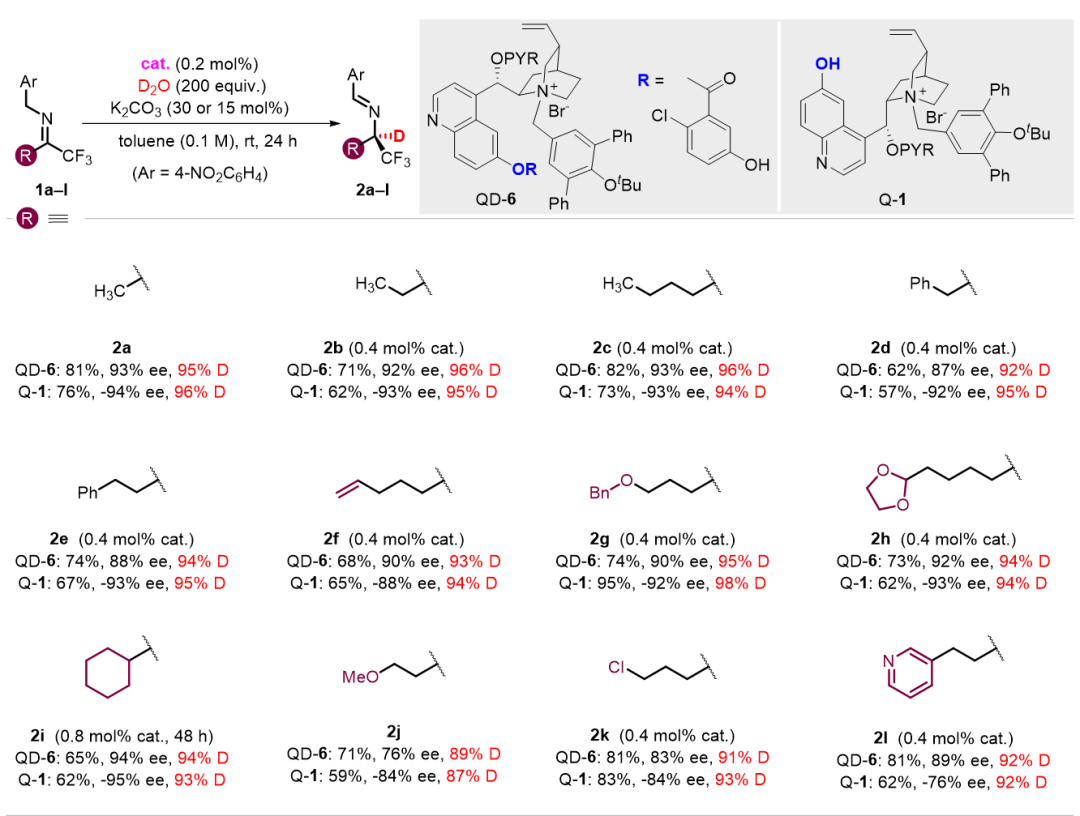
Table 1. 脂肪族三氟甲基亚胺的催化不对称异构化‒氘代反应
针对芳香族三氟甲基亚胺底物,通过对催化剂、溶剂和碱的当量等反应条件的优化,也实现了71-96%的氘代率、62-84%的对映选择性和31-93%的分离产率,且两种对映体产物同样可高效制备,实现了芳香族底物的高效不对称合成(Table 2)。
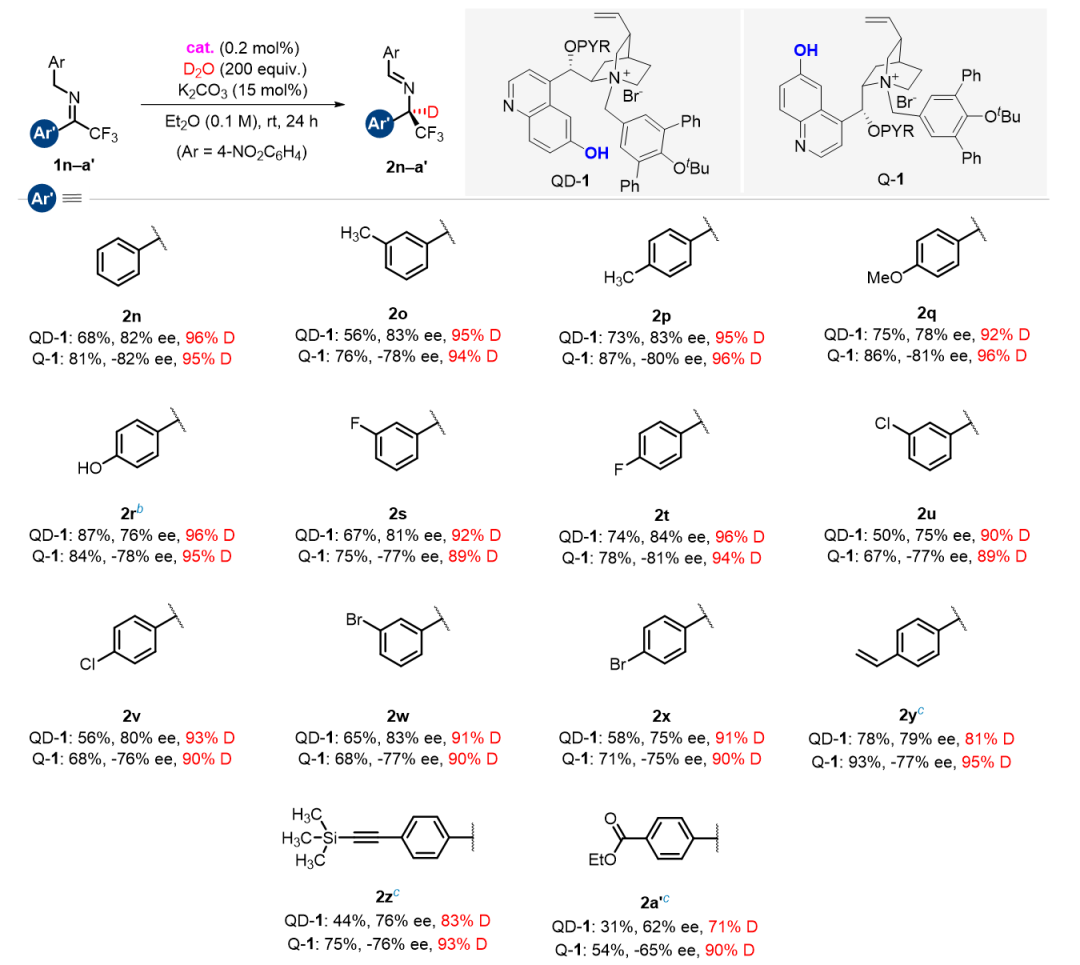
Table 2. 芳香族三氟甲基亚胺的催化不对称异构化‒氘代反应
此外,团队还开发了消旋α-氘代三氟甲基胺的高效合成方法:以三乙胺或四丁基溴化铵为催化剂、重水为氘源,可实现脂肪族和芳香族三氟甲基亚胺的高效异构化‒氘代,氘代率高达91-99%,分离收率71-99%,该方法使用廉价氘源和催化剂、操作简便、条件温和,适合α-氘代三氟甲基胺的规模化制备,为工业级应用奠定了基础(Table 3)。
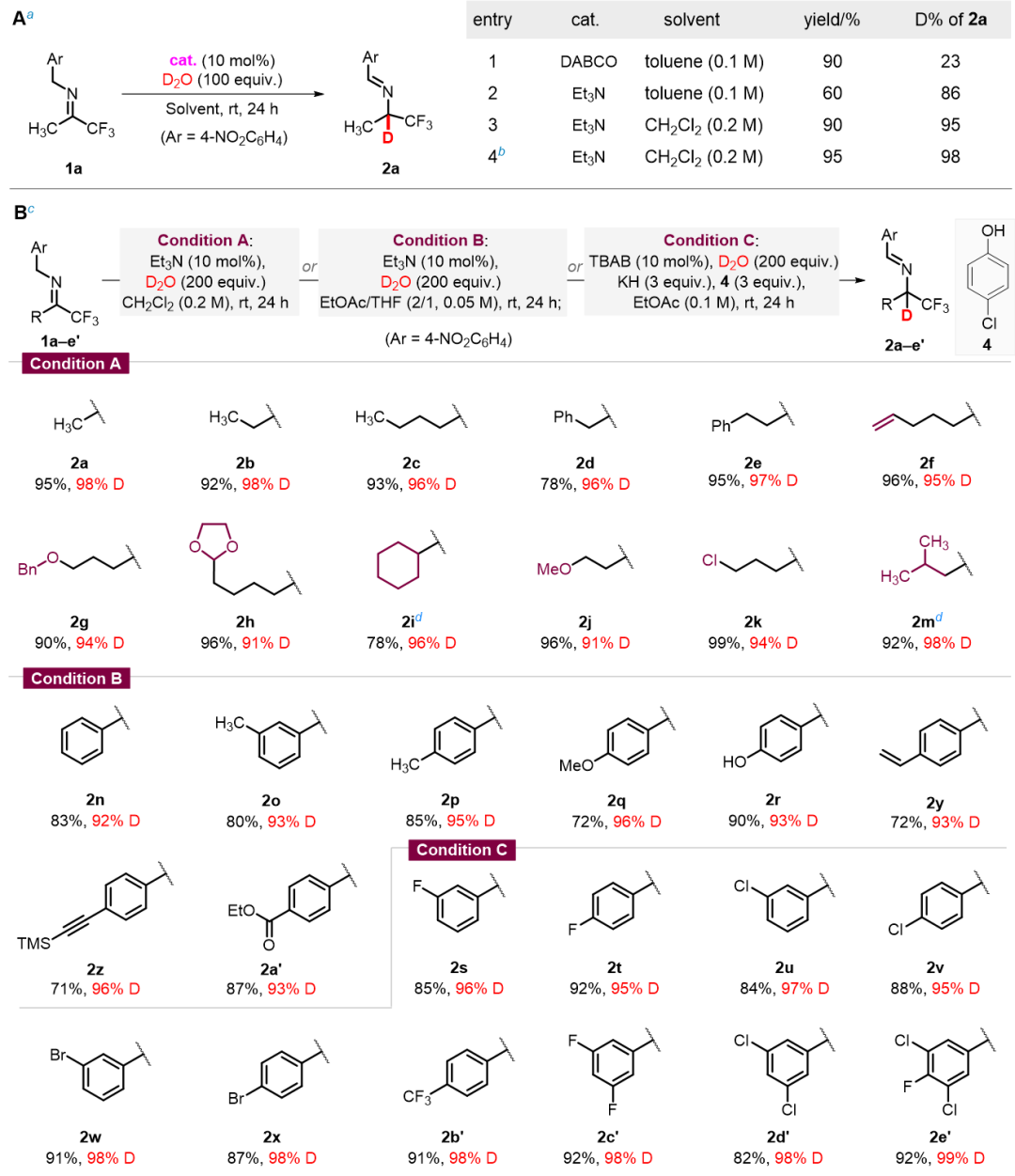
Table 3. 消旋α-氘代三氟甲基胺的合成
研究还验证了该合成方法的应用价值(Figure 1):在1.0 mmol的放大实验中,反应仍能保持95%的氘代率和87%的ee值,展现出良好的放大潜力;产物可通过简单水解直接转化为氘代胺类化合物,且氘代率无损失。团队还以抗炎药物奥沙普秦为原料,通过四步反应将其转化为含手性α-氘代三氟甲基胺基团的衍生物,为药物的氘代化结构改造和氘代药物的创新研发提供了一种可行路径。
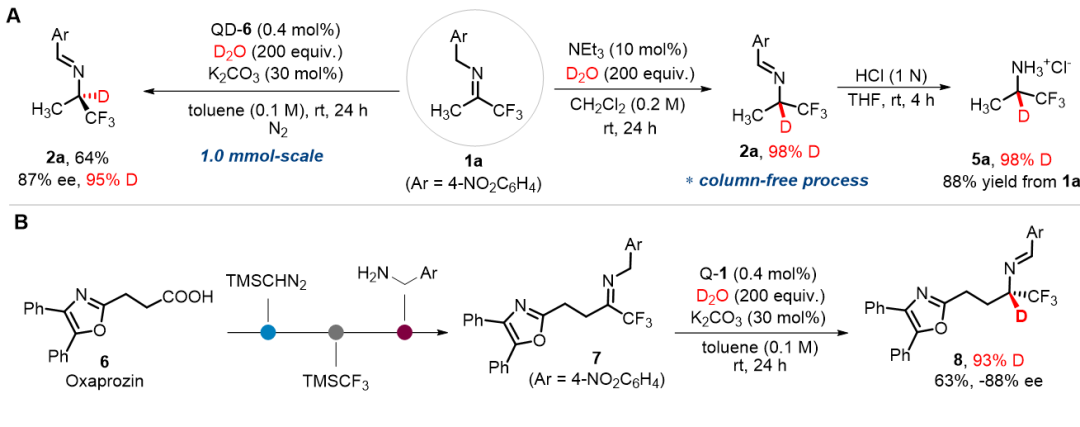
Figure 1. 合成应用
该研究首次实现了以廉价易得的重水为氘源的烷基和芳基α-氘代三氟甲基胺的高效、高选择性合成,该方法具有底物范围广、氘代率高、立体选择性高、成本低廉、操作简便等诸多优势,不仅丰富了氘代化合物的合成方法,也为α-氘代三氟甲基胺在药物研发等领域的应用打开了新空间。同时,该工作基于催化机制指导反应条件优化与催化剂精准设计的研究策略,为深入理解有机小分子催化机制及发展新型催化剂提供了重要参考和有益借鉴。
该研究得到了国家自然科学基金、浙江省领军型创新创业团队、浙江省重点实验室建设项目及西湖大学科研基金的资助。
邓力教授及团队介绍
邓力,西湖大学徐益明讲席教授、副校长、理学院执行院长,自1998年以来致力于不对称有机催化反应及机理研究,通过发展新型高效有机催化剂,建立广谱性的有机催化范式,开发新反应以发展化学合成新策略。
目前,课题组在有机合成化学、不对称催化反应等方向拟招聘博士后3人,科研助理2人。诚挚欢迎对有机化学有浓厚兴趣的青年人才加入。
邮箱:deng_lab@westlake.edu.cn
















